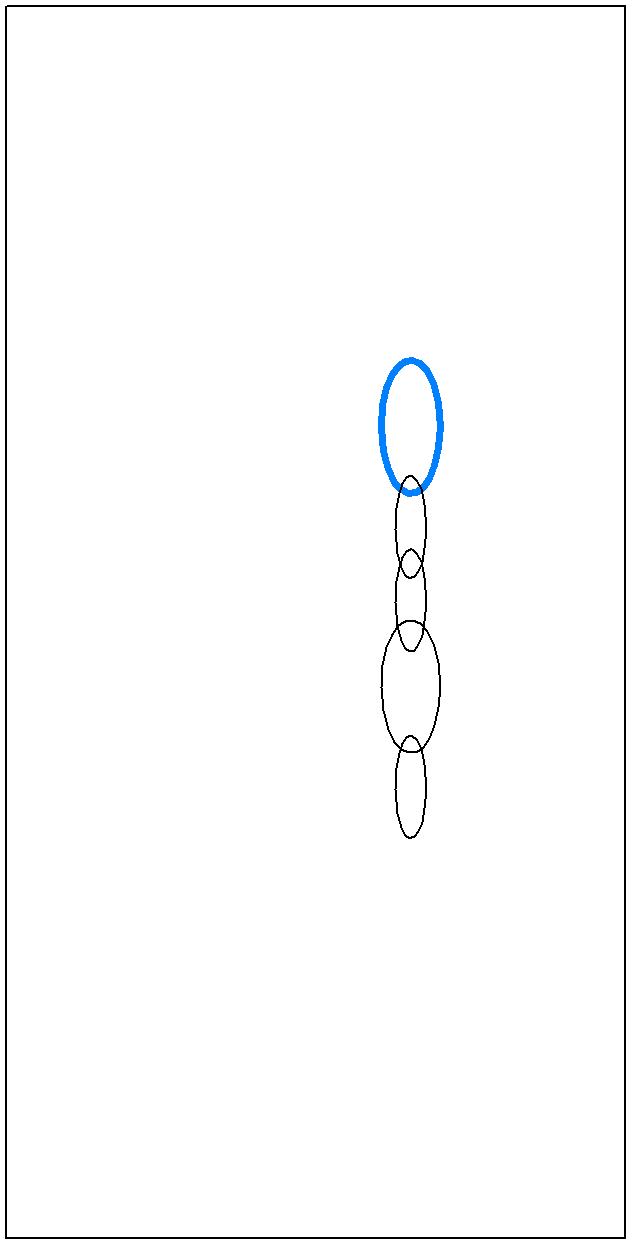
Общепринятая электронная формула
Cl – 1s2 2s2 2p6 3s2 3p5
Cl – [Ne] 3s2 3p5
Изомеры химического элемента
Изомеры химического элемента – Хлор
Свойства химического элемента – Хлор
| Относительная электроотрицательность (по Полингу): | 2,83 |
| Температура плавления: | -100,98°C |
| Температура кипения: | -34,6°C |
| Теплопроводность: | 0 |
| Плотность: | 0,003214 г/см3 |
| Открыт: | Карл Вильем Шееле |
| Цвет в твёрдом состоянии: | Желто-зеленый |
| Тип: | Галоген |
| Орбитали: | 1s22s22p63s23p5 |
| Электронная формула: |
Cl – 1s2 2s2 2p6 3s2 3p5 Cl – [Ne] 3s2 3p5 |
| Валентность: | -1, +1, (+2), +3, (+4), +5, +7 |
| Степени окисления: | -I, 0, +I, III, IV, V, VI, VII |
| Сверхпроводящее состояние при температуре: | 0 К |
| Потенциалы ионизации: | 12,967 В 23,81 В 39,611 В |
| Электропроводность в тв. фазе: | |
| Ковалентный радиус: | 0,99 Å |
| Атомный объем: | 22,7 см3/моль |
| Атомный радиус: | 0,97 Å |
| Теплота распада: | 3,203 КДж/моль |
| Теплота парообразования: | 10,2 КДж/моль |
| Кристаллическая структура: | Орторомбическая. Все углы прямые. Имеется по атому в каждой вершине |
Изотопы химического элемента – Хлор
| Символ нуклида |
Z(p) | N(n) | Масса изотопа (а. е. м.) |
Период полураспада (T1/2) |
Спин и чётность ядра |
|---|---|---|---|---|---|
| Энергия возбуждения | |||||
| 28Cl | 17 | 11 | 28,02851 | 1+ | |
| 29Cl | 17 | 12 | 29,01411 | 20,0 нс | 3/2+ |
| 30Cl | 17 | 13 | 30,00477 | 30 нс | 3+ |
| 31Cl | 17 | 14 | 30,99241 | 150 мс | 3/2+ |
| 32Cl | 17 | 15 | 31,985690 | 298,0 мс | 1+ |
| 33Cl | 17 | 16 | 32,9774519 | 2,511 с | 3/2+ |
| 34Cl | 17 | 17 | 33,97376282 | 1,5264 s | 0+ |
| 34mCl | 146,36 кэВ | 32,00 мин | 3+ | ||
| 35Cl | 17 | 18 | 34,96885268 | стабилен | 3/2+ |
| 36Cl | 17 | 19 | 35,96830698 | 301 тыс. лет | 2+ |
| 37Cl | 17 | 20 | 36,96590259 | стабилен | 3/2+ |
| 38Cl | 17 | 21 | 37,96801043 | 37,24 мин | 2- |
| 38mCl | 671,361 кэВ | 715,0 мс | 5- | ||
| 39Cl | 17 | 22 | 38,9680082 | 55,6 мин | 3/2+ |
| 40Cl | 17 | 23 | 39,97042 | 1,35 мин | 2- |
| 41Cl | 17 | 24 | 40,97068 | 38,4 с | 1/2+ |
| 42Cl | 17 | 25 | 41,97325 | 6,8 с | |
| 43Cl | 17 | 26 | 42,97405 | 3,07 с | 3/2+ |
| 44Cl | 17 | 27 | 43,97828 | 560 мс | |
| 45Cl | 17 | 28 | 44,98029 | 400 мс | 3/2+ |
| 46Cl | 17 | 29 | 45,98421 | 232 мс | |
| 47Cl | 17 | 30 | 46,98871 | 101 мс | 3/2+ |
| 48Cl | 17 | 31 | 47,99495 | 100 мс | |
| 49Cl | 17 | 32 | 49,00032 | 50 мс | 3/2+ |
| 50Cl | 17 | 33 | 50,00784 | 20 мс | |
| 51Cl | 17 | 34 | 51,01449 | 2 мс | 3/2+ |